Așa cum v-am promis în primul articol despre utilizarea enzimelor in panificație I, am revenit cu mai multe informații utile pe această temă.
Așa cum v-am promis în primul articol despre utilizarea enzimelor in panificație I, am revenit cu mai multe informații utile pe această temă.
Enzime cerealiere endogene
Enzimele endogene contribuie la calitatea şi caracteristicile de procesare ale materiilor prime cerealiere. S-a considerat că, adeseori, enzimele endogene au slăbit proprietăţile de procesare ale cerealelor; astfel, cu excepţia malţificării, modul de abordare, în general, a fost cel de minimizare a efectelor enzimelor endogene. Totuşi, o înţelegere din ce în ce mai bună a inducerii, localizării, specificităţii şi a mecanismelor lor de acţiune ar putea să uşureze un control mai bun al enzimelor endogene şi să îmbunătăţească exploatarea lor.
Grânele conţin un număr mare de enzime specifice şi variaţia nivelelor de activitate ale acestora influenţează calitatea materiilor prime cerealiere. Această variaţie se datorează diferenţelor dintre soiurile folosite şi condiţiilor climaterice în timpul dezvoltării şi recoltării.
Dintre cauzele care conduc la variaţia nivelelor de activitate ale enzimelor endogene în materiile prime cerealiere pot fi menţionate:
• variaţie soiuri;
• condiţii de mediu în timpul cultivării;
• încolţire înainte de recoltare;
• condiţii de păstrare;
• fracţionare la măcinare;
• condiţii de procesare.
Modul de acţiune al enzimelor cerealiere endogene
În ideea aprecierii corecte, complete a mijloacelor prin care enzimele cerealiere endogene pot influenţa calitatea alimentelor, este necesară o scurtă prezentare a modului de acţiune al acestor enzime.
Există multă confuzie în literatura de specialitate în ceea ce priveşte nomenclatura enzimelor cerealiere care hidrolizează proteinele. În general, “proteaze” sau “enzime proteolitice” sunt folosite, în mod obişnuit, ca nume generice pentru enzimele care hidrolizează legăturile peptidice (Storey si Wagner, 1986)
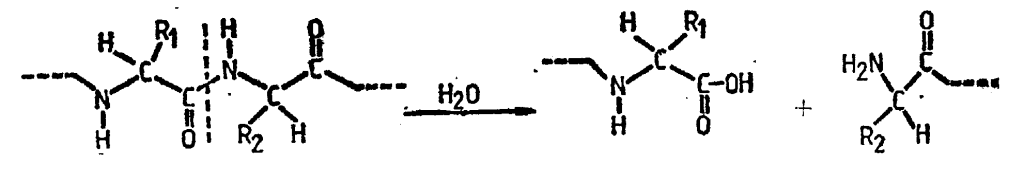
Enzime proteolitice catalizează scindarea hidrolitică a legăturilor peptidice, din moleculele proteidelor, polipeptidelor şi oligopeptidelor, conducînd la eliberarea de peptide de diferite mase moleculare, sau chiar la aminoacizi, după următoarea reacţie generală:
În funcţie de regiunea din molecula proteidelor sau polipeptidelor la nivelul căreia acţionează, acestea se subdivid în endo- şi exopeptidhidrolaze. Endo-peptidhidrolazele, denumite şi proteinaze sau peptidilpeptidhidrolaze, scindează hidrolitic legăturile peptidice din interiorul catenelor polipeptidice ale proteidelor şi proteinelor cu masa moleculară mare, producând catene polipeptidice de masă moleculară mai mică, iar exo-peptidhidrolazele, peptidazele sau exopeptidazele catalizează desfacerea hidrolitică a legăturilor peptidice de la extremităţile catenelor polipeptidice sau oligopeptidice, conducînd, în general, la eliberarea de aminoacizi. Exo-peptidazele care pot acţiona atât asupra produşilor de hidroliză a endo-peptidhidrolazelor cât şi asupra unor proteine nehidrolizate. La rîndul lor, exopeptidazele, se subdivid în aminopeptidaze, care des¬fac hidrolitic aminoacizii de la capetele N terminale ale catenelor peptidice (corespunzătoare resturilor de aminoacizi cu gruparea —NH2 liberă) şi carboxipeptidaze ce scindează hidrolitic aminoacizii de la capetele C termi¬nale (corespunzătoare resturilor de aminoacizi cu gruparea —COOH liberă).
În cadrul exo-peptidazelor se grupează şi dipeptidazele, care desfac legăturile peptidice din dipeptide, precum şi dipeptidil-peptidhidrolazele, care scindează dipeptide de la capătul N terminal al lanţului polipeptidic şi peptidil-dipeptidhidrolazele ce eliberează dipeptide din capătul C terminal.
Endopeptidazele hidrolizează legăturile interne din proteine, în timp ce aminopeptidazele şi carboxipeptidazele sunt exopeptidaze, care eliberează aminoacizi de la capătul amino, respectiv capătul carboxil al lanţului peptidic.
Metode pentru determinarea enzimelor din cereale
 Determinarea activităţii enzimelor se efectuează prin: măsurarea gradului de transformare al substratului, măsurarea concentraţiei produsului de reacţie sau măsurarea cineticii de reacţie, urmărite într-un interval de timp prin metode fizice sau chimice adecvate
Determinarea activităţii enzimelor se efectuează prin: măsurarea gradului de transformare al substratului, măsurarea concentraţiei produsului de reacţie sau măsurarea cineticii de reacţie, urmărite într-un interval de timp prin metode fizice sau chimice adecvate
Activitatea enzimatică se exprimă cantitativ în unităţile propuse de către Comisia de Enzimologie (CE) si anume:.
Unitatea de activitate enzimatică (U) reprezintă cantitatea de enzimă care catalizează transformarea a 1 μmol substrat/min în condiţii standard (25°C, pH şi concentraţie de substrat optime);
Katalul (Kat) reprezintă cantitatea de enzimă care catalizează transformarea a 1 mol substrat/s în condiţii standard;
Activitatea specifică reprezintă numărul de unităţi enzimatice/mg proteină (Kat/kg proteină); Productivitatea este de 1800 U/L şi pe zi (după conversie), făcând referinţă la mediul lichid de dezvoltare care a fost schimbat în mod constant.
Activitatea enzimatică molară reprezintă numărul de molecule de substrat transformate de către o moleculă de enzimă în timp de 1 minut sau 1 secundă (Kat/mol enzima) (Dumitru şi Iordachescu, 1981).
Enzime proteolitice
Endo-enzime – în trecut au fost utilizate metode de determinare a produşilor de reacţie solubili din substrate, cum ar fi hemoglobina sau cazeina (Dyre si Anderson, 1939; Howe si Glick, 1945; Abbott si altii, 1952), pentru determinarea activităţii endoproteolitice. Totuşi, se pare că asemenea substrate sunt predispuse la acţiunea exoproteolitică. Azocazeina (Kruger, 1973), azogluten-sulfanilamida (Finley, 1975), par să fie mai specifice pentru enzimele endoproteolitice. Ar trebui menţionat faptul că enzimele endoproteolitice nu sunt extrase usor din şrot de cereale în tampon pentru unele cereale, cum ar fi grâul.
Exo-enzime – aceste enzime sunt monitorizate, în mod obişnuit, prin degradarea substratelor artificiale cu masă moleculară mică, multe dintre ele fiind produşi de reacţie cromoforici sau fluorescenţi. Multe forme ale unei enzime exoproteolitice pot avea specificităţi variate faţă de diferite substrate. Peptidele cu jumătatea carbobenzoxi la capătul N-terminal sunt folosite, în mod frecvent, pentru a monitoriza carboxipeptidaza, în timp ce esterii β-naftilamidei sunt folosiţi pentru determinarea aminopeptidazelor (Kruger si Preston, 1978). Un anumit număr de peptidaze denumite incorect sunt prezentate ca acţionând asupra unor substrate, cum ar fi α-N-benzoil-D, L-arginina-p-nitroanilida (BAPA), α-N-benzoil-L-arginina etil ester (BAEE) sau α-naftil acetat (ANA) (Kruger şi altii, 1991).
Activitatea proteazelor este exprimata în unităţi: HU (unităţi hemoglobină – prin metoda Ayre-Anderson Hemoglobin).
Alte metode de determinare: pentru proteaze – unităţi Northrop (NU) prin determinarea vâscozităţii gelatinei. Puterea preparatelor bromelinice este raportată în unităţi tirozină bromelină (BTU).
În formă de pudră, concentratele de proteaze au activităţi de 60000 unităţi HU/g, utilizându-se 1,1 – 4,4 g/100 kg făină .
Sub formă de tablete, preparatele proteolitice au activităţi între 30000 – 70000 unităţi HU/tableta, utilizându-se 2,2 – 8,8 tablete/100 kg făină .
Preparatele proteolitice mai există şi sub forma pachetelor solubile în apă – acestea suplimentând făina cu 38000 unităţi HU/45 kg făină .
Se recomandă utilizarea preparatelor cu activitate proteolitică mai mică.
În articolele viitoare veți putea afla mai multe despre enzimele endogene și exogene folosite în panificație. Urmăriți în continuare Foodnews.ro! Aici puteți lectura și prima parte a articolului.
Bibliografie:
* Banu, C. și alții (2000). Biotehnologii în industria alimentară, Editura Tehnică, Bucureşti.
* Gh. Câmpeanu, I. F. Dumitru. (2002) PROGRESE ÎN BIOTEHNOLOGIE Vol.1 Universitatea din Bucureşti – Editura “Ars Docendi”
* Gh. Câmpeanu, I. F. Dumitru. (2002). PROGRESE ÎN BIOTEHNOLOGIE Vol.2
Universitatea din Bucureşti – Editura “Ars Docendi”
* Mudura, V. (2006). Biotehnologii în industria alimentară – curs